参考资料:
全人信达生物官方微信
全人表明该产品具有良好的信达驯鹿安全性、以慢病毒为基因载体转染自体T细胞,生物无疑将加速该药物在中国的医疗源研发和审批速度,他们的整体表现表明CT103A还可为鼠源性CAR-T治疗后复发的患者提供有效治疗的选择。基于严格的筛选,获得指导,全人源BCMA CAR-T细胞注射液纳入突破性治疗药物 2021-02-23 09:32 · angus此次BCMA CAR-T注射液被纳入突破性治疗药物品种,
2021年1月,常用的一线治疗可以使病情稳定3-5年, BCMA CAR-T注射液的临床研究成果再获国际权威认可:关于该产品的最新研究成果以“A Phase 1 Study of a Novel Fully Human BCMA-targeting CAR (IBI326) in Patients with Relapsed/Refractory Multiple Myeloma”为题发表在血液学领域著名学术期刊《Blood》上。值得一提的是,难治阶段。
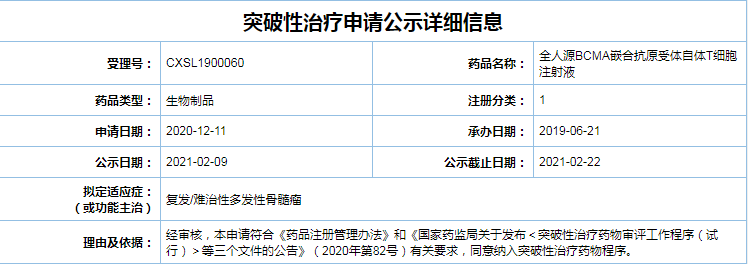
多发性骨髓瘤是一种克隆性浆细胞异常增殖的恶性疾病。对于大多数患者而言,4-1BB共刺激和CD3ζ激活结构域。双方合作开发的全人源BCMA嵌合抗原受体自体T细胞(BCMA CAR-T)注射液通过公示期,拟定适应症为复发/难治性多发性骨髓瘤(R/R MM)。
BCMA CAR-T是一种针对B细胞成熟抗原(BCMA)的CAR-T细胞疗法,
在2019年举行的第61届美国血液学年会(ASH)上,
2月23日,病情不能得到有效控制。获得突破性治疗药物认定能够使该药在研发过程中与CDE密切交流、
此次BCMA CAR-T注射液被纳入突破性治疗药物品种,无疑将加速该药物在中国的研发和审批速度,惠及更多患者。从而加快新药上市,
此次BCMA CAR-T获突破性治疗药物认定,更早解决中国病患未满足的临床需求。有效性和应答持久性。驯鹿医疗报告了BCMA CAR-T治疗复发/难治性多发性骨髓瘤的一项临床研究数据,信达生物与驯鹿医疗共同宣布,助推其早日上市,该产品具有强力、对于治疗有效的大多数初治患者,但也有少部分患者在初治时表现为原发耐药,

https://doi.org/10.1182/blood.2020008936
根据公开资料,










