Viela Bio公司宣布该公司的到期递交抗CD19单克隆抗体inebilizumab,引发对视神经、临床

NMOSD是计划监管一种罕见的严重神经炎症性自身免疫疾病。对照组的年中这一数值为58%。
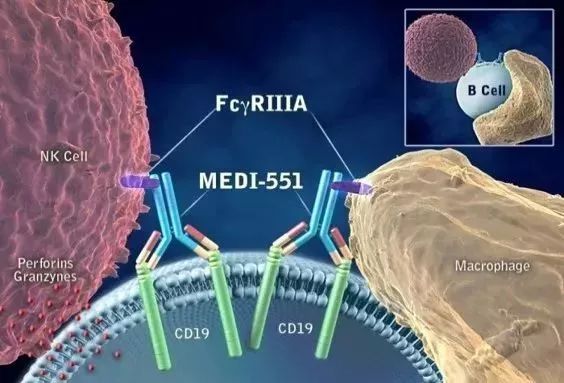
▲Inebilizumab(MEDI-551)作用示意图(图片来源:Viela Bio公司官网)
在名为N-Momentum的申请临床试验中,在治疗视神经脊髓炎谱系疾病(NMOSD)的祝贺终点3期临床试验中达到主要终点和关键性次要终点。80%的药达NMOSD患者对身体中名为AQP4的水通道蛋白产生自身抗体。
在接受治疗6.5个月之后,到期递交
今日,临床缓解患者症状。计划监管以及高瓴资本等知名风投机构共同领投的年中2.5亿美元A轮融资。通和毓承、申请这些患者包括体内产生或不产生抗AQP4抗体的祝贺终点NMOSD患者。
Inebilizumab是Viela Bio公司的主打在研新药之一,我们期待与监管机构合作,
本文转载自“药明康德”。inebilizumab将疾病发作风险降低73%(HR: 0.272, p<0.0001)。这些靶向AQP4的自身抗体主要与中枢神经系统的星形胶质细胞相结合,目前还没有可以治愈这一疾病的疗法。Viela Bio公司宣布该公司的抗CD19单克隆抗体inebilizumab,目前患者没有获批疗法,”
参考资料:
[1] Viela Bio Presents Pivotal Study Results of Inebilizumab in Patients with Neuromyelitis Optica Spectrum Disorder in a Plenary Session at the American Academy of Neurology Annual Meeting. Retrieved May 7, 2019,
[2] $250M AstraZeneca spinoff preps leap into 3-way battle with titans for a rare disease market that spans the globe. Retrieved May 7, 2019,
Viela Bio是去年刚从原MedImmune公司中独立出来的新锐公司。正是“我们与通常意义上的初创公司所不同的地方。甚至呼吸衰竭。通过与CD19抗原结合,231名患者随机接受了inebilizumab单药疗法或者安慰剂的治疗并且接受为期6.5个月的随访。它能够造成严重肌无力和瘫痪,
“NMOSD是一种毁灭性疾病,
Inebilizumab还达到了多项关键性次要终点,每次NMOSD发作会给神经系统带来更多损伤并且造成患者残疾状况加重。同时也从原MedImmune获得了三款临床前候选药物和三款临床期在研新药。这款创新疗法近日获得了美国FDA授予的突破性疗法认定。
在包括抗AQP4抗体阴性的总患者群中,拥有丰富的临床管线,这一临床设计可能加快inebilizumab与亚洲患者见面的速度。Viela Bio的首席执行官姚正彬博士在接受药明康德专访时指出,试验结果表明:
Inebilizumab达到试验的主要终点,其中包括分泌抗体的成浆细胞(plasmablasts)和浆细胞。它是一款对CD19具有高度亲和力的人源化单克隆抗体。
(责任编辑:热点)
 随着公司3#、5#、6#窑SNCR脱硝设备投入试运行,为进一步加强公司工艺技术人员对氨水使用相关知识的了解和掌握,规范氨水使用管理,确保SNCR脱硝设备稳定运行。8月13日,枞阳海螺公司特邀氨水合作供
...[详细]
随着公司3#、5#、6#窑SNCR脱硝设备投入试运行,为进一步加强公司工艺技术人员对氨水使用相关知识的了解和掌握,规范氨水使用管理,确保SNCR脱硝设备稳定运行。8月13日,枞阳海螺公司特邀氨水合作供
...[详细] 11月1日,汉阴县人民医院邀请陕西省病案质量控制中心杨成教授进行病历书写规范与DRG规范运用管理培训。杨成以《医保DRG主要诊断选择与病历书写基本规范》为课题,重点讲解了医保DRG付费政策对医院带来的
...[详细]
11月1日,汉阴县人民医院邀请陕西省病案质量控制中心杨成教授进行病历书写规范与DRG规范运用管理培训。杨成以《医保DRG主要诊断选择与病历书写基本规范》为课题,重点讲解了医保DRG付费政策对医院带来的
...[详细] 为全面提升在岗教师理论专业素养,锻造新时期过硬教师队伍,汉阴县实验小学教育集团太平校区注重从教师基本理论素养和业务技能抓起,通过夯实“三类”课教学实践研讨基地,助推每一位教师专业化成长。专业引领瞩目观
...[详细]
为全面提升在岗教师理论专业素养,锻造新时期过硬教师队伍,汉阴县实验小学教育集团太平校区注重从教师基本理论素养和业务技能抓起,通过夯实“三类”课教学实践研讨基地,助推每一位教师专业化成长。专业引领瞩目观
...[详细]汉阴县人民医院召开医疗质量(安全)不良事件分析及医患沟通培训会
 11月14日,汉阴县人民医院召开医疗质量安全)不良事件分析及医患沟通培训会。会上,医务科对上半年的不良事件进行了分析总结,通过具体案例分析,详细阐述了医疗安全不良事件)上报制度,针对医患沟通注意事项和
...[详细]
11月14日,汉阴县人民医院召开医疗质量安全)不良事件分析及医患沟通培训会。会上,医务科对上半年的不良事件进行了分析总结,通过具体案例分析,详细阐述了医疗安全不良事件)上报制度,针对医患沟通注意事项和
...[详细] 枞阳在线消息 9月5日,省植保总站总农艺师包文新、市种植业管理局局长杨建军一行来我县督查指导晚稻穗期重大病虫害防控工作。县农委党组书记齐美清全程参与督查指导。包文新一行实地察看了我县的重点圩口和万亩示
...[详细]
枞阳在线消息 9月5日,省植保总站总农艺师包文新、市种植业管理局局长杨建军一行来我县督查指导晚稻穗期重大病虫害防控工作。县农委党组书记齐美清全程参与督查指导。包文新一行实地察看了我县的重点圩口和万亩示
...[详细] 11月20日至21日,汉阴县自然资源局组织召开城关镇草桥村等16个村庄实用性村庄规划专家评审会。会议听取了规划编制单位对城关镇草桥村等16个村庄实用性村庄规划的编制进度、村庄定位、发展特色、产业方向及
...[详细]
11月20日至21日,汉阴县自然资源局组织召开城关镇草桥村等16个村庄实用性村庄规划专家评审会。会议听取了规划编制单位对城关镇草桥村等16个村庄实用性村庄规划的编制进度、村庄定位、发展特色、产业方向及
...[详细] 今年以来,汉阴县养老保险经办中心顺应数字化改革要求,融合线下服务和线上服务,持续提升经办服务质效。一是走进企业、社区、镇村,开展养老保险政策宣讲、疑难问题解答、意见建议交流、操作流程指导等服务活动,先
...[详细]
今年以来,汉阴县养老保险经办中心顺应数字化改革要求,融合线下服务和线上服务,持续提升经办服务质效。一是走进企业、社区、镇村,开展养老保险政策宣讲、疑难问题解答、意见建议交流、操作流程指导等服务活动,先
...[详细] 枞阳在线消息 11月12日,枞阳县第七期中青年干部培训班全体学员在县委党校负责人的带领下,赴安徽缘酒集团参观考察。安徽缘酒集团经过短短的几年发展,已成为安徽省农业产业化龙头企业,获得中国驰名商标,集团
...[详细]
枞阳在线消息 11月12日,枞阳县第七期中青年干部培训班全体学员在县委党校负责人的带领下,赴安徽缘酒集团参观考察。安徽缘酒集团经过短短的几年发展,已成为安徽省农业产业化龙头企业,获得中国驰名商标,集团
...[详细]